Salpeterzuur: De Procesreacties

![]()
In blok 1, de convertor, wordt ammoniak verbrand in aanwezigheid van een katalysator waarbij NO ontstaat. De katalysator die nodig is moet regelmatig vervangen worden en is erg duur. Waarom wordt de katalysator niet achterwege gelaten om zo kosten te besparen?
|
Zonder katalysator verbrandt NH3 niet.
| |
|
Zonder katalysator verbrandt NH3 explosief.
| |
|
Zonder katalysator ontstaat er N2 en H2O.
| |
|
Zonder katalysator ontstaat er NO3-
en H3O+.
|
 De reactie die plaatsvindt in blok 1 kan worden
weergegeven met de volgende reactievergelijking. Maak deze kloppend.
De reactie die plaatsvindt in blok 1 kan worden
weergegeven met de volgende reactievergelijking. Maak deze kloppend.
NH3(g) +
O2(g) →
NO(g) +
H2O(l)
 In blok 2 wordt stikstofmonooxide met extra zuurstof
omgezet in stikstofdioxide volgens onderstaande reactievergelijking. Maak weer
kloppend.
In blok 2 wordt stikstofmonooxide met extra zuurstof
omgezet in stikstofdioxide volgens onderstaande reactievergelijking. Maak weer
kloppend.
NO(g) +
O2(g) →
NO2(g)
 Het ontstane stikstofdioxide zou in evenwicht zijn met
distikstoftetraoxide. Dit evenwicht zou aflopend zijn door de verdere omzetting
van het distikstoftetraoxide naar salpeterzuur door extra water en zuurstof via
deze reactievergelijking. Maak maar weer eens kloppend.
Het ontstane stikstofdioxide zou in evenwicht zijn met
distikstoftetraoxide. Dit evenwicht zou aflopend zijn door de verdere omzetting
van het distikstoftetraoxide naar salpeterzuur door extra water en zuurstof via
deze reactievergelijking. Maak maar weer eens kloppend.
N2O4 +
H2O
+
O2 →
HNO3
 Deze reactievergelijking is om een aantal redenen
onbevredigend. Bedenk samen met een andere leerling, twee redenen en noteer
deze in je labjournaal.
Deze reactievergelijking is om een aantal redenen
onbevredigend. Bedenk samen met een andere leerling, twee redenen en noteer
deze in je labjournaal.![]()
Als je na vijf
minuten er nog niet uit bent vraag dan een hint aan de PAL.
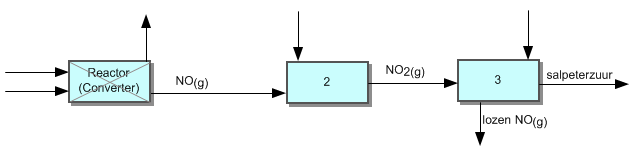
 In het filmpje wordt in de laatste stap van het
productieproces het stikstofmonooxide uit het salpeterzuur verwijdert door
lucht door te blazen en dit gecontroleerd te lozen aan de lucht. Bedenk samen
met die andere leerling, twee redenen waarom dit beter kan en noteer deze in je
labjournaal.
In het filmpje wordt in de laatste stap van het
productieproces het stikstofmonooxide uit het salpeterzuur verwijdert door
lucht door te blazen en dit gecontroleerd te lozen aan de lucht. Bedenk samen
met die andere leerling, twee redenen waarom dit beter kan en noteer deze in je
labjournaal.![]()
Ook hier geldt dat als je er na vijf minuten niet uit bent, je de PAL voor een hint kunt vragen.
 Aan de genoemde bezwaren kan tegemoet gekomen worden
door uit te gaan van de volgende reactievergelijking. Maak deze kloppend.
Aan de genoemde bezwaren kan tegemoet gekomen worden
door uit te gaan van de volgende reactievergelijking. Maak deze kloppend.
NO2(g) +
H2O(l)
→
H3O+(aq)
+
NO3-(aq)
+
NO(g)
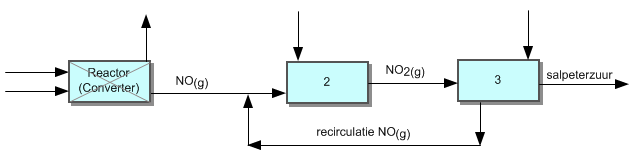
 Het stikstofmonooxide kan ook oplossen in water en
vervolgens reageren tot salpeterigzuur. Maar het kan ook, zoals in het filmpje
genoemd, uit de oplossing verwijderd worden en teruggeleid in het proces,
gerecirculeerd. Met een kleine aanpassing zou het blokschema er dan zoals
hieronder uit komen te zien. Dit incomplete blokschema staat in je labjournaal en kun je daar aanvullen.
Het stikstofmonooxide kan ook oplossen in water en
vervolgens reageren tot salpeterigzuur. Maar het kan ook, zoals in het filmpje
genoemd, uit de oplossing verwijderd worden en teruggeleid in het proces,
gerecirculeerd. Met een kleine aanpassing zou het blokschema er dan zoals
hieronder uit komen te zien. Dit incomplete blokschema staat in je labjournaal en kun je daar aanvullen.![]()